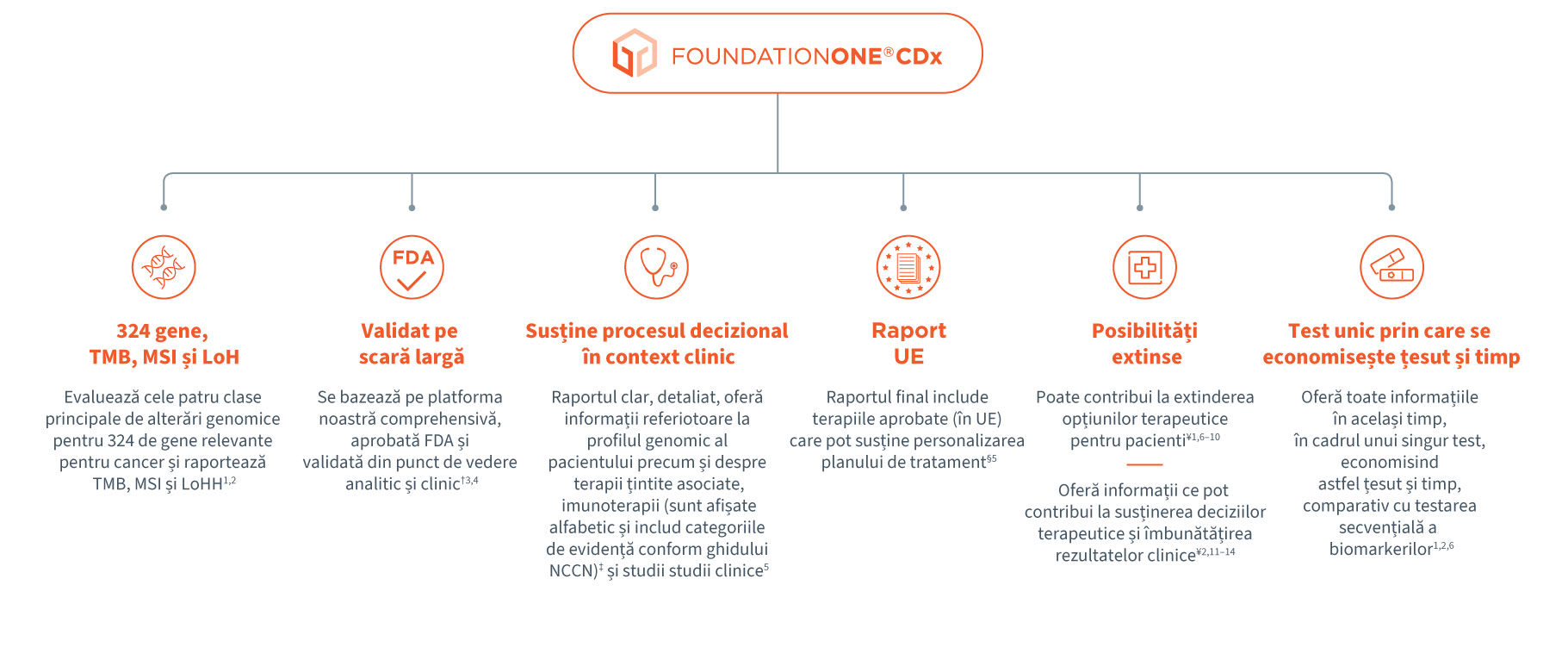
*Substituții de baze, inserții si deleții, alterări ale numarului de copii si rearanjări de gene.
†Validarea clinică a demonstrat concordanța cu următoarele teste companion: test cobas® de mutație EGFR, test Ventana ALK (D5F3) CDx, Vysis ALK Break-Apart FISH Probe Kit, therascreen® KRAS RGQ PCR Kit, Dako HER2 FISH PharmDx® Kit, test cobas® de mutație BRAF V600, kit THxID® BRAF. Pentru mai multe informații, vă rugăm să consultați Informațiile tehnice FoundationOne®CDx disponibile la: www.rochefoundationmedicine.com/f1cdxtech
‡Pentru informații suplimentare despre categoriile NCCN, vă rugăm să consultați NCCN Compendium® (www.nccn.org).
§Terapiile conținute în versiunea UE a raportului pot fi aprobate printr-o procedură centralizată a UE sau printr-o procedură națională într-un stat membru al UE.
EGFR, epidermal growth factor receptor (receptor pentru factorul de crestere epidermal); FDA, US Food and Drug Administration; FISH, fluorescence in situ hybridisation (Hibridizare prin fluorescență in situ); LoH, Loss of Heterozygosity (Pierderea heterozigozității); IHC, Immunohistochemistry (Imunohistochimie); MSI, Microsatellite Instability (Instabilitate microsatelitară); NCCN, National Comprehensive Cancer Network; NGS, Next Generation Sequencing (Secvențiere de nouă generație); NSCLC, non-small cell lung cancer (Cancer de plămân altul decât cel cu celule mici); PARP, poly-ADP ribose polymerase; PD-L1, programmed cell death ligand 1 (Ligandul 1 pentru moarte celulară programată); TKI, tyrosine kinase inhibitor (Inhibitori de tirozin-kinază); TMB, Tumour Mutational Burden (Încarcatură mutaționala tumorală).